Ein Expertenausschuss der Europäischen Arzneimittelagentur EMA hat den Weg für zwei an die Omikron-Variante angepasste von Biontech/Pfizer sowie von Moderna freigemacht. Das teilte die EMA am Donnerstagnachmittag mit. Die EU-Kommission muss nun noch formal über die Zulassung entscheiden. Laut EMA wurde die Zulassung für Menschen ab zwölf Jahren empfohlen, welche zumindest gegen grundimmunisiert sind.
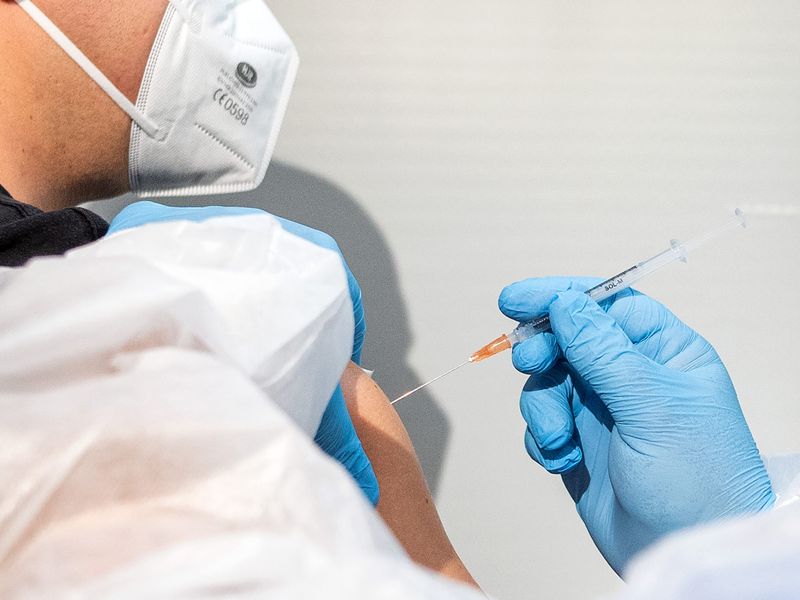
EMA empfahl Zulassung von Omikron-Vakzinen gegen Corona
1-09-2022, 15:05
EMA empfahl die Zulassung von Omikron-Vakzinen gegen Corona
Wie ein Sprecher der EU-Kommission sagte, werde die Brüsseler Behörde die Entscheidung der EMA sehr schnell annehmen. Ob dies noch am gleichen Tag geschehe, sei aber offen. Die EMA-Entscheidung betrifft Anträge von Biontech/Pfizer und des US-Unternehmens Moderna auf Zulassung von sogenannten bivalenten mRNA-Impfstoffen, die vor dem ursprünglichen Sars-CoV-2 und vor der Omikron-Sublinie BA.1 Schutz bieten sollen. In Österreich oder Deutschland spielen diese Viren mittlerweile keine Rolle mehr. Die Hoffnung ist aber, dass dieser Impfstoff auch gegen die aktuell kursierenden Omikron-Sublinien besser wirkt.
EMA und EU-Kommission öffneten damit Weg für weitere Impfkampagnen
Mit der Entscheidung der EMA und der EU-Kommission ist der Weg frei für die Fortsetzung der Impfkampagnen. Österreichs Nationales Impfgremium (NIG) hat am gestrigen Mittwoch die Corona-Auffrischungsimpfung für alle Menschen ab zwölf Jahren empfohlen. Bisher galt die Empfehlung für den vierten Stich für Menschen ab 60 Jahren. Nachdem nun am Donnerstag wie erwartet der speziell für die Omikron-Variante BA.1 angepasste Impfstoff von EMA grünes Licht bekommen hat, soll dann einige Wochen später der an die aktuelle Variante BA.4/BA.5 angepasste Impfstoff folgen.
(APA/Red)




